a. Les analgésiques ou morphiniques
Les morphiniques ou analgésiques sont injectés lors d’une anesthésie générale pour éliminer toute forme de sensation douloureuse.
Lors d’une anesthésie générale, la morphine et les dérivés morphiniques sont les plus utilisés.
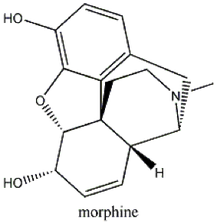
La morphine a pour formule brute: C17H19NO3. La masse molaire moléculaire de la morphine est 285g/mol.
- Les médicaments utilisés
Lors d’une anesthésie générale, la morphine et les dérivés morphiniques sont les plus utilisés.
La morphine a pour formule brute: C17H19NO3. La masse molaire moléculaire de la morphine est 285g/mol.
 (Wikipédia)
(Wikipédia)
Elle provient du pavot à opium. A partir de cette plante, lorsque les capsules ne sont pas mûres, est extrait le suc, appelé l’opium. Il contient des alcaloïdes dont 10% de morphine. L’opium est utilisé depuis les débuts pour soulager l’homme de la douleur. En 1805, F. Sertuner découvre le principe actif de l’opium et le nomme « morphine » en référence à Morphée, dieu grec des rêves, en pensant surement à l’euphorie qu’entraine la morphine. C’est donc au XIXe siècle qu’on extrait pour la première fois les alcaloïdes présents dans ce suc pour les utiliser dans la médecine grâce à leurs vertus pourtant bien connues depuis des millénaires ! Ce sont des molécules organiques contenant au moins un atome de carbone lié avec au moins un atome d’hydrogène, elles sont azotées, de caractère basique. Elles ont une forme presque toujours hétérocyclique. La morphine est directement présente dans l’opium de façon naturelle, c’est un opiacé.
Il existe beaucoup d’autres molécules opiacées telles que la codéine, la narcotine, ou encore l’hydromorphone, l’oxymorphone… dont certaines sont aussi utilisées pour l’anesthésie générale pour leurs vertus analgésiques.
Les autres opiacés utilisés dans l’anesthésie générale sont les dérivés morphiniques. Il s’agit des agonistes morphiniques. Les voici (leur demi-vie allant de 3, 7 heures à 9 minutes) : fentanyl, sufentanil, alfentanil et rémifentanil.
Ces opiacés agissent sur le système nerveux central. Ainsi, ils ont un effet analgésique et certains sont capables d’avoir un effet analgésique mais aussi hypnotique (voir I. 3) b.). La morphine est capable de produire ces deux effets.
Dans le cadre d’une anesthésie générale, elle est utilisée pour ses vertus analgésiques car ses vertus hypnotiques ne sont pas suffisantes pour bien endormir le patient.
Pour comprendre le mode d’action de la morphine ainsi que des autres médicaments (hypnotiques et curares) injectés (que l’on expliquera dans le I. 3) b. et le I. 3) c.), il faut comprendre les mécanismes liés à la douleur.
Les autres opiacés utilisés dans l’anesthésie générale sont les dérivés morphiniques. Il s’agit des agonistes morphiniques. Les voici (leur demi-vie allant de 3, 7 heures à 9 minutes) : fentanyl, sufentanil, alfentanil et rémifentanil.
Ces opiacés agissent sur le système nerveux central. Ainsi, ils ont un effet analgésique et certains sont capables d’avoir un effet analgésique mais aussi hypnotique (voir I. 3) b.). La morphine est capable de produire ces deux effets.
Dans le cadre d’une anesthésie générale, elle est utilisée pour ses vertus analgésiques car ses vertus hypnotiques ne sont pas suffisantes pour bien endormir le patient.
Pour comprendre le mode d’action de la morphine ainsi que des autres médicaments (hypnotiques et curares) injectés (que l’on expliquera dans le I. 3) b. et le I. 3) c.), il faut comprendre les mécanismes liés à la douleur.
- Le message douloureux
Un stimulus douloureux ou des stimuli douloureux sont à l’origine de la sensation de douleur que l’on peut exprimer. Il existe une très grande quantité de stimuli différents qui peuvent se manifester d’un simple coup ou alors de traumatismes, de torsions, de compressions, de brûlures. A partir du stimulus, un circuit assez complexe sera mis en place jusqu’à la perception du cerveau et la réaction comportementale face à la douleur.
|
Lorsque la puissance de certains stimuli dépasse un certain seuil, les nocicepteurs (terminaisons nerveuses libres) et les récepteurs (par exemple ceux du toucher) sont activés mais cela peut se faire de manière directe ou indirecte. Directe lorsqu’un nocicepteur ou récepteur est directement touché ou indirecte lorsqu’un stimulus douloureux engendre la libération de substances algésiogènes des cellules de la peau qui activent les nocicepteurs ou récepteurs. Il faut que plusieurs nocicepteurs ou récepteurs reçoivent le stimulus douloureux en même temps pour que le message douloureux soit en pris en compte.
|
|
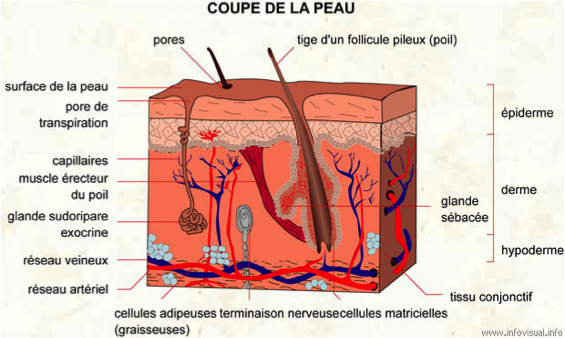
Au niveau cutané, les nocicepteurs sont en très grand nombre et recouvrent même tout le territoire cutané de l’organisme, ils se situent dans l’épiderme ou le derme, ce qui explique pourquoi la sensibilité est plus importante et plus précise au niveau cutané.
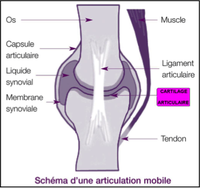
Au niveau musculaire, les nocicepteurs sont moins nombreux et répartis de façon espacée, ainsi la douleur est moins facilement localisable. Au niveau vasculaire, les nocicepteurs sont nombreux au niveau des parois externes ainsi que les récepteurs nerveux, ce qui permet de réguler la pression artérielle à l’aide d’une boucle de régulation nerveuse qui sera mise en place. Au niveau des tissus osseux, les terminaisons libres se situent dans la moelle épinière, donc un stimulus douloureux ne peut être ressenti que lors d’une fracture par exemple. Aux articulations, les nocicepteurs sont répartis dans la capsule, la synoviale, les ligaments et les tendons. Au niveau viscéral, les nocicepteurs sont répartis de façon inégale et sont moins nombreux pour les organes creux (tube digestif, voies urogénitales), la sensation de douleur est vague et se localise difficilement. Pour les organes pleins (poumons, reins, rate et foie), les nocicepteurs sont également en faible quantité, ainsi ces organes sont peu sensibles face à la douleur. |
|
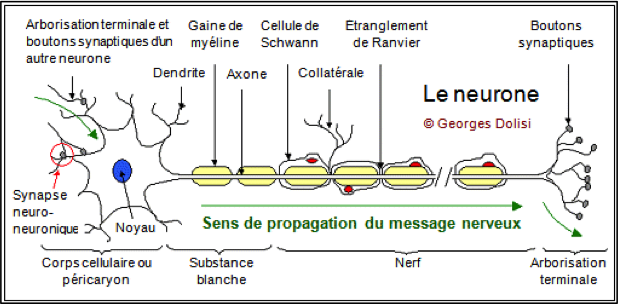
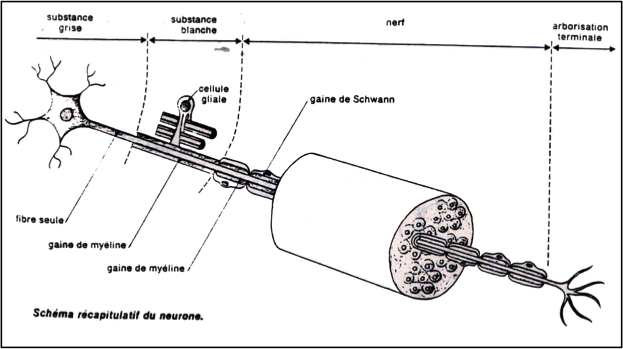
Il faut avant tout savoir que les nocicepteurs sont rattachés à des fibres nerveuses qui forment les nerfs. Une fibre nerveuse est constituée d’un neurone et de son axone ainsi que des terminaisons libres. Les nocicepteurs, sous l’effet des substances algésiogènes, vont alors développer un influx nerveux qui va se propager jusqu’à la moelle épinière tout le long d’une fibre nerveuse.
Il existe différents types de fibres nerveuses qui transmettent le message douloureux : - Les fibres Aα ont le plus gros diamètre (entre 6 et 17 µm) transmettent l’influx nerveux plus rapidement. - Les fibres Aδ sont plus fines (entre 1 et 5 µm) et véhiculent les messages moins rapidement, à une vitesse de 20 m/s. - Les fibres C sont très fines (entre 0,3 et 1,5 µm) et conduisent les potentiels d’action plus lentement, à une vitesse de 2m/s. Lorsque les terminaisons libres sont stimulées, elles vont alors créer un influx nerveux, ce qui correspond à la création de potentiels d’action tout le long de la fibre nerveuse. En effet, les fibres nerveuses alors stimulées se dépolarisent puis se polarisent, c’est-à-dire que leurs signaux électriques deviennent positifs puis négatifs à nouveau en une milliseconde. |
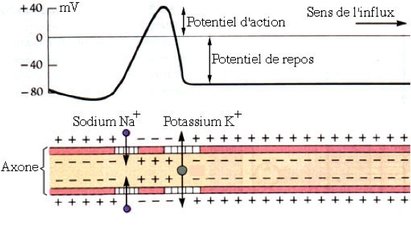
Le potentiel d’action (PA) :
La membrane du neurone possède une pompe à protéines ainsi que des canaux à Na+ et à K+. Avant que le neurone soit dépolarisé par l’influx nerveux, ce dernier est au repos, c’est-à-dire que les ions sodiums et potassiums sont inégalement partagés de part et d’autre de la membrane. C’est un partage maintenu par la pompe à ions sodium et potassium : les ions sodiums sont majoritairement placés dans le milieu extracellulaire (à l’extérieur de la membrane) alors que les ions potassium sont retenus dans le cytoplasme de la membrane. On trouve, plus précisément, dix fois plus d’ions Na+ dans le cytoplasme et vingt fois plus d’ions K+ dans le milieu extracellulaire. Ainsi, au repos, le neurone est polarisé, l’intérieur de la membrane est, en effet, plus négatif que le milieu extracellulaire (on a moins de charges positives dans la membrane que dans le liquide extracellulaire). Lorsque parvient l’influx nerveux, la membrane est déséquilibrée et les canaux à sodium s’ouvrent : ils laissent passer les ions sodiums dans la membrane. La membrane devient moins négative, cette partie de fibre est alors dépolarisée, c’est la création d’un potentiel d’action. Ce phénomène de dépolarisation s’accentue une fois les canaux à sodium fermés : les canaux à potassium s’ouvrent et laissent s’échapper les ions potassium dans le milieu intracellulaire en trop grande quantité. Ainsi, une inversion des charges s’effectue : la charge du milieu intracellulaire devient plus basse que celui de la membrane neurone, c’est une hyperpolarisation. Pour rétablir le partage de départ, la pompe va ramener les ions sodium à l’extérieur du neurone et les ions potassium à l’intérieur du neurone. Ainsi, le neurone polarisé s’est dépolarisé en passant par l’hyperpolarisation pour, ensuite, revenir à sa situation initiale, la polarisation : c’est de cette manière que le message nerveux est véhiculé tout le long de la fibre.
On calcule l’intensité du message douloureux grâce à la fréquence des potentiels d’action (PA) : plus il y a de PA, plus le message douloureux est intense.
La membrane du neurone possède une pompe à protéines ainsi que des canaux à Na+ et à K+. Avant que le neurone soit dépolarisé par l’influx nerveux, ce dernier est au repos, c’est-à-dire que les ions sodiums et potassiums sont inégalement partagés de part et d’autre de la membrane. C’est un partage maintenu par la pompe à ions sodium et potassium : les ions sodiums sont majoritairement placés dans le milieu extracellulaire (à l’extérieur de la membrane) alors que les ions potassium sont retenus dans le cytoplasme de la membrane. On trouve, plus précisément, dix fois plus d’ions Na+ dans le cytoplasme et vingt fois plus d’ions K+ dans le milieu extracellulaire. Ainsi, au repos, le neurone est polarisé, l’intérieur de la membrane est, en effet, plus négatif que le milieu extracellulaire (on a moins de charges positives dans la membrane que dans le liquide extracellulaire). Lorsque parvient l’influx nerveux, la membrane est déséquilibrée et les canaux à sodium s’ouvrent : ils laissent passer les ions sodiums dans la membrane. La membrane devient moins négative, cette partie de fibre est alors dépolarisée, c’est la création d’un potentiel d’action. Ce phénomène de dépolarisation s’accentue une fois les canaux à sodium fermés : les canaux à potassium s’ouvrent et laissent s’échapper les ions potassium dans le milieu intracellulaire en trop grande quantité. Ainsi, une inversion des charges s’effectue : la charge du milieu intracellulaire devient plus basse que celui de la membrane neurone, c’est une hyperpolarisation. Pour rétablir le partage de départ, la pompe va ramener les ions sodium à l’extérieur du neurone et les ions potassium à l’intérieur du neurone. Ainsi, le neurone polarisé s’est dépolarisé en passant par l’hyperpolarisation pour, ensuite, revenir à sa situation initiale, la polarisation : c’est de cette manière que le message nerveux est véhiculé tout le long de la fibre.
On calcule l’intensité du message douloureux grâce à la fréquence des potentiels d’action (PA) : plus il y a de PA, plus le message douloureux est intense.
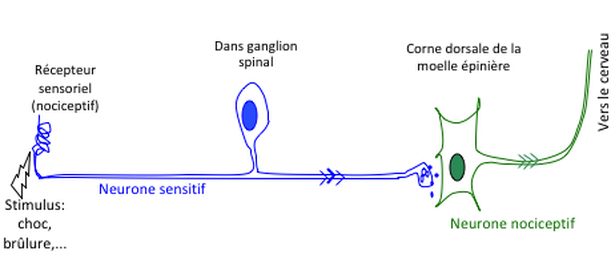
Donc, la stimulation des nocicepteurs produit un influx nerveux qui va, en premier lieu, être véhiculé par le neurone sensitif. L’influx correspond à un potentiel d’action qui voyage tout le long de l’axone. En plus, sa vitesse est accélérée grâce aux nœuds de Ravier présents sur l’axone.
En fonction de l’intensité du message douloureux, les fibres du nerf sont sollicitées, ce qui permettra, plus tard, de différencier l’intensité de la douleur : si ce n’est qu’une sensation tactile, douloureuse ou douloureuse intense. En effet, les fibres Aδ véhiculent un message douloureux intense et ce message arrive en premier, ensuite, le message porté par la fibre C qui correspond à une douleur moins intense, plus sourde et qui dure plus longtemps, arrive au deuxième temps.
Les fibres se prolongent jusque dans la corne postérieure de la moelle épinière en passant par un ganglion des racines dorsales (= ganglions spinaux) où se situe le neurone (le corps cellulaire) de la fibre. Au niveau de la corne postérieure, la fibre qui a, jusqu’ici, véhiculé le message, se termine par une synapse. Le message douloureux va alors être relayé soit au neurone spinal (ou nociceptif), et/ou au nerf moteur, sous forme de neurotransmetteur.
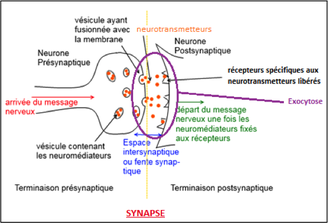
Au niveau de la synapse, se trouvent le neurone pré-synaptique (ici, le neurone sensitif) et le neurone post-synaptique (soit l’inter-neurone (qui transmettra à son tour le message au neurone relié au nerf moteur), soit le neurone nociceptif). Les neurones post-synaptiques sont constitués de récepteurs, il en existe plusieurs types avec des formes différentes, ce qui permettra aux neurotransmetteurs venant du neurone pré-synaptique de se fixer au bon récepteur qui leur est accordé. Les neurotransmetteurs véhiculent des messages entre neurones mais peuvent avoir deux fonctions différentes : certains vont exciter le neurone pour faire passer l’influx nerveux alors que d’autres peuvent inhiber le passage de l’influx nerveux. Ils véhiculent de neurones en neurones au niveau des synapses, en passant du neurone pré-synaptique au neurone post-synaptique par la fente synaptique (très mince de l’ordre de 0, 02 µm).
Les neurotransmetteurs sont regroupés dans plusieurs vésicules synaptiques au sein du neurone pré-synaptique. La membrane du neurone possède également des canaux à calcium (Ca2+). Ces canaux s’ouvrent lorsque l’influx nerveux arrive au niveau du bouton terminal et laissent entrer les ions calciums présents dans l‘environnement du neurone. La quantité de calcium présente dans la synapse du neurone augmente et provoque une dépolarisation pré-synaptique (l’intérieur de la membrane est plus positif que l’extérieur). Cela entraine le déplacement des vésicules séminales vers la membrane. Une fois collées à la membrane du neurone pré-synaptique, se produit l’exocytose des vésicules : elles libèrent les neurotransmetteurs dans la fentesynaptique.
Les neurotransmetteurs traversent la fente synaptique et se fixent aux récepteurs de la membrane du neurone post-synaptique. Ces récepteurs sont des canaux ioniques à ions sodiums (Na+). Lorsque la quantité de neurotransmetteurs est suffisante pour activer les récepteurs, ces derniers s’ouvrent pour laisser passer les ions sodiums et les neurotransmetteurs dans la membrane du neurone post-synaptique.
Avant d’entrer dans la membrane du neurone post-synaptique, la charge de la partie externe du neurone était plus positive et la charge de la partie interne était plus négative car il y a moins d’ions positifs qu’à l’extérieur de la membrane. Avec la pénétration d’ions, se produit une dépolarisation du neurone post-synaptique, c’est-à-dire que les charges seront inversées : la partie externe de la membrane du neurone est alors devenue plus négative et, sa partie interne, plus positive car il y aura plus d’ions positifs dans le neurone post-synaptique qu’à l’extérieur. Si le seuil est atteint dans le neurone post-synaptique, un influx sera alors produit : la membrane du neurone créé un potentiel électrique qui se propage jusqu’au prochain neurone, c’est la transmission de l’influx nerveux.
Les neurotransmetteurs sont regroupés dans plusieurs vésicules synaptiques au sein du neurone pré-synaptique. La membrane du neurone possède également des canaux à calcium (Ca2+). Ces canaux s’ouvrent lorsque l’influx nerveux arrive au niveau du bouton terminal et laissent entrer les ions calciums présents dans l‘environnement du neurone. La quantité de calcium présente dans la synapse du neurone augmente et provoque une dépolarisation pré-synaptique (l’intérieur de la membrane est plus positif que l’extérieur). Cela entraine le déplacement des vésicules séminales vers la membrane. Une fois collées à la membrane du neurone pré-synaptique, se produit l’exocytose des vésicules : elles libèrent les neurotransmetteurs dans la fentesynaptique.
Les neurotransmetteurs traversent la fente synaptique et se fixent aux récepteurs de la membrane du neurone post-synaptique. Ces récepteurs sont des canaux ioniques à ions sodiums (Na+). Lorsque la quantité de neurotransmetteurs est suffisante pour activer les récepteurs, ces derniers s’ouvrent pour laisser passer les ions sodiums et les neurotransmetteurs dans la membrane du neurone post-synaptique.
Avant d’entrer dans la membrane du neurone post-synaptique, la charge de la partie externe du neurone était plus positive et la charge de la partie interne était plus négative car il y a moins d’ions positifs qu’à l’extérieur de la membrane. Avec la pénétration d’ions, se produit une dépolarisation du neurone post-synaptique, c’est-à-dire que les charges seront inversées : la partie externe de la membrane du neurone est alors devenue plus négative et, sa partie interne, plus positive car il y aura plus d’ions positifs dans le neurone post-synaptique qu’à l’extérieur. Si le seuil est atteint dans le neurone post-synaptique, un influx sera alors produit : la membrane du neurone créé un potentiel électrique qui se propage jusqu’au prochain neurone, c’est la transmission de l’influx nerveux.
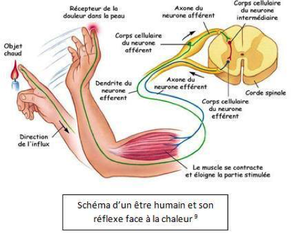
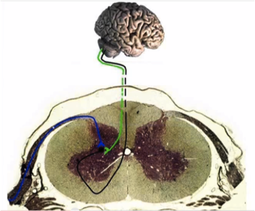
Au niveau de cette synapse, le message peut être relayé à une des fibres motrices du nerf moteur (en bleu) en lien avec les muscles en passant par un inter-neurone (en rouge), ce dernier sera à l’origine d’un réflex (par exemple, on ôte la main de la source de douleur).
Le message douloureux est aussi relayé au neurone nociceptif. Il permet de remonter l’influx nerveux au cerveau, le long de sa fibre qui lui est associée, via le tronc cérébral qui va alors accélérer le cœur.
Au niveau de la moelle épinière, la fibre sensitive mise en jeu se termine par une synapse. Le message nerveux est alors transmis sous forme de neurotransmetteurs à la fibre nociceptive qui véhiculera le message nerveux au cerveau, soit à un inter-neurone qui transmettra à son tour le message au nerf moteur qui provoquera un réflex.
L’influx nerveux parvient au thalamus qui transmet, à son tour, l’information au cortex cérébral. Le cortex cérébral est capable de localiser et de caractériser la douleur grâce à une de ses régions qui est le cortex somesthésique.
Le système limbique recevra aussi les informations du message douloureux, il est impliqué dans les émotions, les comportements et la mémorisation.
L’hypothalamus et l’hypophyse vont sécréter des endorphines ou des endomorphines (dont les enképhalines) qui se dispersent dans le système nerveux central. Ces substances chimiques calment naturellement la douleur lorsqu’elle est trop forte mais ne sont pas suffisantes pour supprimer la douleur que le patient ressentira lors d’une opération.
Le système limbique recevra aussi les informations du message douloureux, il est impliqué dans les émotions, les comportements et la mémorisation.
L’hypothalamus et l’hypophyse vont sécréter des endorphines ou des endomorphines (dont les enképhalines) qui se dispersent dans le système nerveux central. Ces substances chimiques calment naturellement la douleur lorsqu’elle est trop forte mais ne sont pas suffisantes pour supprimer la douleur que le patient ressentira lors d’une opération.
Le cheminement des messages nerveux se fait donc par polarisation et dépolarisation successif du neurone de la fibre sensitive (qui remonte l’information à la moelle épinière), de celui de la fibre nociceptive (qui va remonter l’information au cerveau) et/ou de celui du nerf moteur (qui provoquera un réflex).
Comment le corps humain est-il capable d’atténuer la douleur naturellement ?
Les enképhalines ont pour rôle d’inhiber le message nerveux, elles ont deux actions pour arriver à leur but. Elles se fixent, en effet, sur les récepteurs opioïdes présents dans la moelle épinière (kappa et delta) et au cerveau (mu). En se fixant sur les récepteurs présents au niveau de la moelle épinière, elles atténuent la douleur ; en se fixant au niveau du cerveau, elles augmentent la libération de dopamine. La dopamine est un neurotransmetteur qui contribue à la sensation de plaisir. Cette deuxième action des enképhalines n’est pas liée à l’atténuation de la douleur. C’est pourquoi cela ne sera pas expliqué plus précisément. ( voir plus bas le mode d’action de la morphine )
Les enképhalines ont pour rôle d’inhiber le message nerveux, elles ont deux actions pour arriver à leur but. Elles se fixent, en effet, sur les récepteurs opioïdes présents dans la moelle épinière (kappa et delta) et au cerveau (mu). En se fixant sur les récepteurs présents au niveau de la moelle épinière, elles atténuent la douleur ; en se fixant au niveau du cerveau, elles augmentent la libération de dopamine. La dopamine est un neurotransmetteur qui contribue à la sensation de plaisir. Cette deuxième action des enképhalines n’est pas liée à l’atténuation de la douleur. C’est pourquoi cela ne sera pas expliqué plus précisément. ( voir plus bas le mode d’action de la morphine )
|
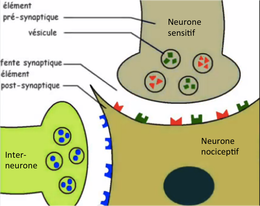
Fixation des enképhalines aux récepteurs opioïdes de la moelle épinière :
Le cerveau transmet les enképhalines qui sont les endorphines à la moelle épinière grâce à l’inter-neurone (en vert) qui se finit par une synapse (voir schémas). Ce sont des neurotransmetteurs que les neurones au niveau du cerveau libèrent lorsque la sensation douloureuse est trop intense. Donc, le rôle des enképhalines est d’inhiber les potentiels d’action, ils ont un effet analgésique. Au niveau de cette synapse, il y a transmission du message nerveux, on a donc : le neurone sensitif excité qui transmet ses neurotransmetteurs vers le neurone nociceptif. Ces neurotransmetteurs se fixent sur les récepteurs du neurone nociceptif post-synaptique. Ainsi, le neurone nociceptif créé à son tour un potentiel d’action qu’on appelle potentiel d’action post-synaptique (PPS). Ce PPS va permettre au neurone de créer un nouveau PA. Lorsque le message douloureux est fort, le cerveau peut l’inhiber grâce à l’inter-neurone. Cet inter-neurone a le même fonctionnement que les autres neurones, c’est-à-dire qu’il est excité lorsque le message douloureux est important, il créé des PA, sauf que les neurotransmetteurs qu’il lâchera lors de l’exocytose au niveau de la synapse sont spéciaux : ce sont les enképhalines. Les enképhalines se fixent sur les récepteurs opioïdes kappa et delta du neurone post-synaptique (le neurone nociceptif) qui est déjà excité. Leur fixation entraine la création d’un PPS dans le neurone post-synaptique. Ce dernier vient s’opposer à l’autre PPS (expliqué auparavant) crée en même temps. Le PA qui se crée à partir de ces PPS est alors moindre ou peut même être nul. |
Le cerveau est donc capable de sécréter des enképhalines capables d’inhiber en partie la sensation douloureuse en intervenant au niveau de la moelle épinière.
Pour résumer la transmission du message douloureux, nous vous conseillons de visionner la vidéo youtube suivante : https://www.youtube.com/watch?feature=player_detailpage&v=3w-wjZxjmmM
- Le mode d'action des morphiniques
Mise en évidence des effets de la morphine : (les effets de la morphine sont identiques à ceux des autres analgésiques sauf que le délai d’action et la durée d’action sont différentes).
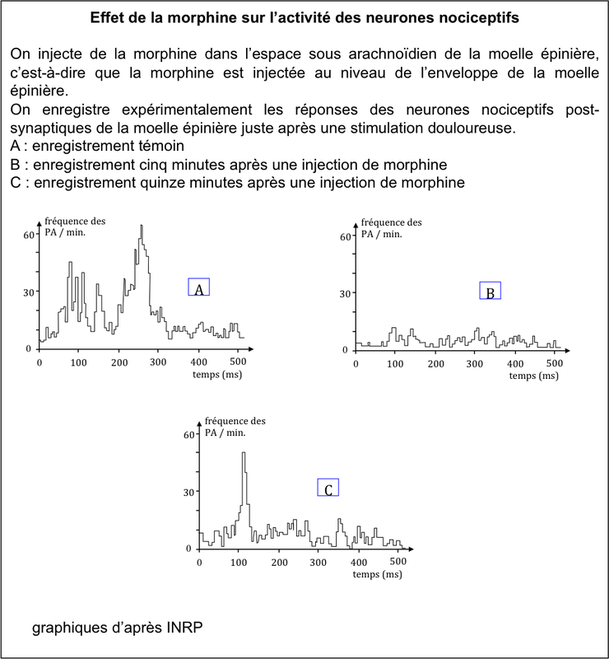
Ces trois graphiques sont issus d’une expérience lors de laquelle les réponses des neurones nociceptifs post-synaptiques de la moelle épinière juste après une stimulation douloureuse ont été enregistrées. Ces réponses sont les potentiels d’action, leur fréquence par minute est ici enregistrée.
L’enregistrement A correspond à l’enregistrement témoin, c’est-à-dire qu’on a enregistré l’activité de ce neurone en temps normal, lorsque celui-ci subit une stimulation douloureuse.
L’enregistrement B a été effectué 5 minutes après l’injection de morphine et l’enregistrement C, 15 min après.
En comparant l’enregistrement A avec l’enregistrement B, la fréquence de potentiel d’action par minute lors d’une stimulation est très faible 5 minutes après injection de morphine.
Pour l’enregistrement C, la fréquence des potentiels d’action augmente 15 minutes après l’injection.
On peut en déduire que la morphine réduit la fréquence de potentiels d’action. De plus, au bout de 15 min, la fréquence de potentiels d’action augmente et va redevenir normale lors d’une stimulation.
Donc, la morphine diminue l’activité des neurones, elle inhibe le message nerveux. L’action de la morphine diminue au bout d’un certain temps, elle a une durée d’action à peu près égale à 15 min (cela dépend de la quantité injectée, de l’analgésique injecté et de la résistance de la personne face aux médicaments), l’activité des neurones redevient ensuite normale.
Comment la morphine bloque-t-elle la transmission du message nerveux ?
La morphine bloque l’influx nerveux qui achemine le message douloureux. Elle a en effet le même mode d’action que les enképhalines (voir la douleur) sauf qu’elle est plus puissante, elle est capable de bloquer l’influx nerveux.
En effet, elle se fixe sur les mêmes récepteurs que les enképhalines situés au niveau de la moelle épinière (les récepteurs Kappa (κ) et Delta (δ)) ainsi qu’au niveau du cerveau (les récepteurs opiacés Mu (μ)). La morphine inhibe alors fortement la transmission du message nerveux entre les nerfs. Nous avons vu que lorsque les enképhalines et donc ou la morphine se fixe sur les récepteurs opioïdes du cerveau, il y a libération de dopamine qui est un acteur de la sensation de plaisir. Dans le cadre d’une anesthésie générale, cet aspect n’intervient pas (c’est pourquoi il n’a pas été expliqué dans l’explication du cheminement du message douloureux) de la morphine n’intervient pas car la personne n’est pas consciente sous l’emprise d’hypnotiques (voir I. 3) b.)
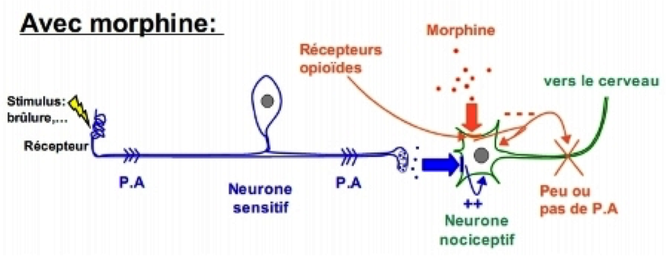
La morphine a donc une action au niveau de la moelle épinière. Lorsqu’elle se fixe sur les récepteurs Kappa et Delta du neurone nociceptif (récepteurs identiques à ceux des enképhalines), elle créé donc aussi un PPS inhibiteur (comme la fixation des enképhalines) mais, cette fois-ci, plus puissant. Donc, les deux PPS (voir la fin de la douleur) (le premier est la transmission du message douloureux et le deuxième est créé par la fixation de la morphine) s’opposent. Comme celui crée par la morphine est plus puissant, la transmission, ensuite sous forme de PA, s’annule complètement (alors que les enképhalines le réduisaient). Ainsi, le message douloureux est complètement inhibé. Cela se traduit par une analgésie et, de plus, le patient ne pourra ressentir de douleur sous l’emprise de morphiniques. Cependant, la fixation sur les récepteurs Delta entraine aussi une dépression respiratoire : elle diminue le rythme et l’amplitude de la respiration. A de trop fortes doses, la morphine peut bloquer la respiration du patient notamment par sa rapidité d’action lors de son injection. Ce risque augmente lors que le patient a des problèmes pulmonaires, neurologiques ou bien lorsque son âge est avancé.
Schéma bilan de l’action de la morphine au niveau de la moelle épinière et conséquence sur les neurones nociceptifs